胃癌中位总生存期18.0个月,靶向+免疫+化疗三联疗法,给CLDN18.2阳性胃癌患者带来新希望
2026年3月16日,在《Nature Medicine》期刊上,发表了佐妥昔单抗(zolbetuximab)联合mFOLFOX6化疗方案和纳武利尤单抗(Nivolumab)一线治疗不可切除的CLDN18.2阳性胃或胃食管结合部腺癌患者的II期ILUSTRO研究队列4的结果[1]。
患者特征
该队列包含两个子队列:4A(安全性导入期)和 4B(扩展期)。队列4B纳入了既往未经治疗、CLDN18.2阳性、HER2阴性的患者。
数据截至2025年9月2日,队列4共入组77例接受了800mg/m²负荷剂量佐妥昔单抗的患者(队列4A,n=6;队列4B,n=71)。患者的中位年龄为61.0岁(范围:37.0-86.0岁),其中62.3%为男性。
65例(85.5%)患者的肿瘤表现为CLDN18.2高表达(≥75%的肿瘤细胞呈现中-强膜性CLDN18染色),11例(14.5%)患者的肿瘤为CLDN18.2中表达(≥50%且<75%的肿瘤细胞呈现中-强膜性CLDN18染色)。
63例(81.8%)患者在基线时具有可测量病灶,且大多数患者(86.5%)的原发肿瘤部位在胃。
在可获得肿瘤PD-L1状态的患者中(n=75),34.7%的患者PD-L1综合阳性评分<1,65.3%的患者CPS≥1。
疗效分析
在队列4B中,中位随访时间为11.5个月,中位无进展生存期(PFS)为14.8个月。6个月和12个月的PFS率分别为72.6%和59.1%。
在CLDN18.2高表达的患者(n=59)中,中位PFS为18.0个月。
在57例CLDN18.2高表达患者中,36例(63.2%)的PD-L1 CPS≥1,中位PFS为23.6个月。而CLDN18.2高表达但PD-L1 CPS<1的患者(n=21)中位PFS为12.1个月。
在分析时,中位总生存期(OS)数据尚未成熟,中位随访时间为15.4个月时,队列4B所有患者的中位OS为18.0个月,而在CLDN18.2高表达的患者中,中位OS尚未成熟。
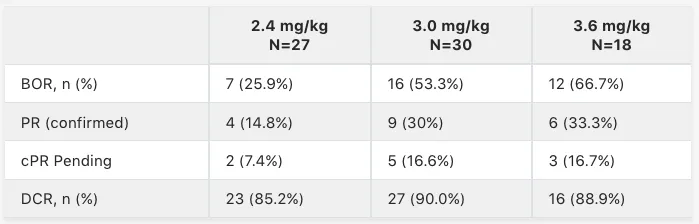
事后分析在基线具有可测量病灶的患者(n=58),客观缓解率(ORR)为62.1%,其中包括2例完全缓解和34例部分缓解,疾病控制率为89.7%。中位缓解持续时间为19.1个月。
在47例基线具有可测量病灶且CLDN18.2高表达的患者中,ORR为68.1%。
在10例基线具有可测量病灶且CLDN18.2中表达的患者中,ORR为40.0%。
在基线具有可测量病灶且CLDN18.2高表达的患者中,对于PD-L1 CPS≥1的患者(n=31),ORR为74.2%。对于PD-L1 CPS<1的患者(n=15),ORR为60.0%。
转移性胃/胃食管结合部腺癌的一线治疗标准是基于铂类/氟尿嘧啶的化疗。在基于铂类/氟尿嘧啶的化疗基础上加入CLDN18.2靶向的治疗可改善患者预后。
CLDN18.2是一种正常表达于胃黏膜细胞的紧密连接蛋白。在恶性转化过程中,这些细胞失去上皮极性,使CLDN18.2的表位暴露于细胞表面,从而为抗体结合提供了治疗靶点。
目前,国内有多个胃癌临床试验进行中,例如:信诺维的CLDN18.2抗体偶联药物XNW27011。

凯石招募——临床试验招募平台
参与临床试验的患者,可以免费用试验新药,与试验相关的检查也是免费的。
目前有CAR-T、TIL等细胞疗法,PD-1/PD-L1等免疫治疗药物,小分子抑制剂、双抗、单抗、ADC等靶向药物的临床试验正在进行中。
正在招募肺癌、食管癌、肝癌、胃癌、结直肠癌、宫颈癌、卵巢癌、乳腺癌、胆管癌、子宫内膜癌、黑色素瘤、肉瘤、恶性血液疾病、淋巴瘤等各种恶性肿瘤,想要了解或者参加临床试验项目,可以咨询我们医学部的老师。

1.Kohei Shitara,Hirokazu Shoj,Nicola Fazio,et al. First-line zolbetuximab plus mFOLFOX6 and nivolumab in unresectable CLDN18.2-positive gastric or gastroesophageal junction adenocarcinoma: a phase 2 trial[J]. Nature Medicine (2026).
2.国家药品监督管理局药品审评中心(CDE)官网.