【招募】免疫治疗,正在改写B细胞急性淋巴细胞白血病的未来——写给每一位正在与B-ALL抗争的患者和家属
近年来,B细胞急性淋巴细胞白血病(B-ALL)的治疗格局正在发生重要变化。传统治疗以强化化疗为主,虽然儿童治愈率已接近90%,但部分高危儿童和成人患者疗效仍不理想,复发后的治疗更加困难。
而现在,一类新的治疗方式——免疫治疗,正以前所未有的速度改变着这一局面,为患者带来新的希望。
今天,我们基于近期发表在《JNCCN》上的一篇重要综述[1],为您系统梳理:目前B-ALL的免疫治疗有哪些?疗效如何?有哪些风险?未来方向是什么?
01|什么是免疫治疗?
免疫治疗,简单来说,就是调动或改造患者自身的免疫系统,使其能够精准识别并清除肿瘤细胞。
在B-ALL中,已经广泛研究和应用的免疫治疗主要分为四大类:
单克隆抗体(mAbs)
抗体-药物偶联物(ADC)
双特异性T细胞衔接抗体(BiTE)
CAR-T细胞治疗
这些疗法大多已经进入临床实践,部分获得FDA批准。
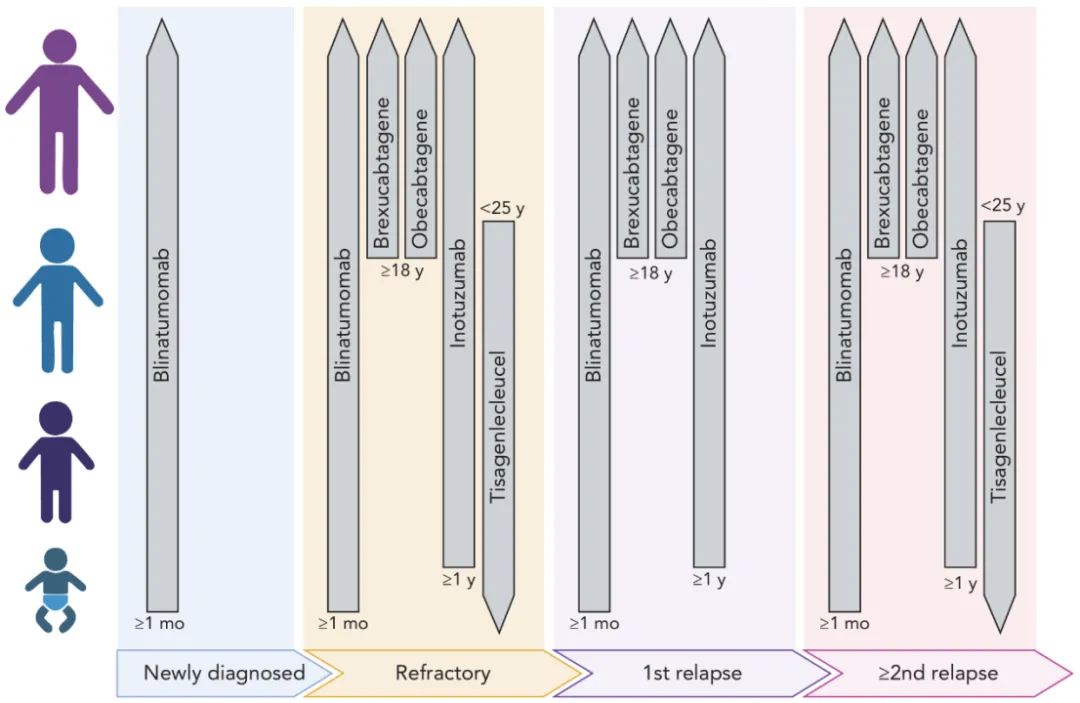
图1 FDA批准的B-ALL免疫疗法概览
02|单克隆抗体:
为部分成人患者带来获益
这类药物能识别并牢牢结合在B-ALL癌细胞的特定蛋白上,相当于给癌细胞贴上一个“快来消灭我”的标签,从而召唤免疫系统的其他细胞前来攻击。
① 代表药物:利妥昔单抗
利妥昔单抗靶向CD20分子,在成人CD20阳性的B-ALL患者中,联合化疗可提高成人患者2年无事件生存率:65%(加入利妥昔单抗)vs 52%(单纯化疗)。
因此,在CD20阳性成人患者中,利妥昔单抗已成为可考虑的诱导治疗组成部分。
但在儿童患者中,研究未显示明确获益,且输注反应发生率较高,因此目前未常规应用于儿童B-ALL。
② 新一代药物:奥法妥木单抗
它在成人中的表现同样亮眼,联合化疗的总反应率高达98%,疗效似乎优于历史数据中的利妥昔单抗。
03|抗体-药物偶联物:
精准“携药”打击肿瘤
这类药物像“定向导弹”,将高效的化疗药物(“弹头”)通过抗体(“导航”)精准地带到癌细胞内部释放,实现定点清除,减少对正常细胞的伤害。
奥加伊妥珠单抗单抗是目前在B-ALL中应用最广泛的ADC之一,靶向CD22,在复发/难治(R/R)患者中的疗效显著。
① 疗效显著
成人患者使用奥加伊妥珠单抗的完全缓解率高达80.7%,远高于传统化疗的29.4%。
在儿童R/R患者的完全缓解率也达到58%-67%,达到缓解的患者中约71%可实现MRD阴性。它已被FDA批准用于≥1岁的复发/难治性B-ALL患者。
在老年或不适合强效化疗的新诊断患者中(该人群传统预后极差,5年总生存率仅23%),使用奥加伊妥珠单抗联合减量化疗的方案取得了令人鼓舞的长期生存数据,5年总生存率可达46%。
② 需要特别注意的风险
感染风险增加(尤其与化疗联合时):在儿童及青少年患者中,将奥加伊妥珠单抗单抗加入强化化疗后,观察到感染并发症增加,影响部分试验进展。
肝窦阻塞综合征(SOS):尤其在后续进行造血干细胞移植时风险增加。
部分老年患者长期随访中出现继发性骨髓恶性肿瘤(目前尚不确定是否与奥加伊妥珠单抗直接相关),因此,医生在使用时会严格评估风险收益。
04|双特异性抗体:
把T细胞“拉过来”杀肿瘤
这类抗体非常巧妙,它有两个“抓手”:一个抓住白血病细胞(CD19),另一个抓住人体自身的免疫T细胞(CD3)。
这样就把T细胞直接拉到癌细胞身边,激活T细胞去杀死癌细胞。代表药物是贝林妥欧单抗,其显著疗效,可以说是目前B-ALL治疗领域的“明星选手”。
① 清除微小残留病
对于化疗后仍有微小残留病阳性的患者,贝林妥欧单抗能使78%的患者转为阴性,显著延长生存期。
② 在复发患者中的疗效
在成人R/R患者中,使用贝林妥欧单抗治疗完全缓解率约43%–56%,在随机对照研究中优于标准化疗。在儿童首次复发患者中,2年无病生存率54.4%(化疗仅39%),总生存率71.3%(化疗仅58.4%)。
③ 在新诊断患者中的突破
一项重要研究显示,在新诊断的成人Ph阴性B-ALL患者中,于化疗巩固阶段加入贝林妥欧单抗,能将3年总生存率从68%大幅提升至85%。
在一项针对初诊标准风险B-ALL儿童患者的大型研究中,加入两个疗程的贝林妥欧单抗后,3年无病生存率高达96%,而单纯化疗组为87.9%。
这项研究因疗效显著而提前结束,并已改变临床实践,使贝林妥欧单抗成为大多数儿童B-ALL的治疗选择。
④ 能否减少化疗?
部分研究显示,在特定人群(如Ph阳性患者)中,使用“类固醇+靶向药+贝林妥欧单抗” 的无化疗诱导方案,已显示出长期且稳定的疗效,部分深度缓解的患者甚至可能无需进行造血干细胞移植,但仍需进一步前瞻性研究确认。
儿童中,对于无法耐受高强度化疗的患儿,用贝林妥欧单抗替代后续化疗也取得了与标准化疗相似的生存率。但目前仍需更多研究验证。
⑤ 常见副作用
主要包括细胞因子释放综合征(CRS)、神经毒性(意识改变、震颤、癫痫等),严重神经毒性发生率通常低于5%。
B细胞发育不良导致的丙种球蛋白低下是其预期内的效应,需要关注和管理。
05|CAR-T治疗:
为复发患者带来革命性突破
这是目前最前沿的免疫疗法之一。它从患者体内提取出T细胞,在实验室里给它们装上能精准识别癌细胞的“导航头”(嵌合抗原受体,CAR),大量扩增后回输到患者体内,精准攻击CD19阳性白血病细胞。
① 靶向CD19的CAR-T细胞:
代表产品有tisagenlecleucel(用于儿童和年轻成人),brexucabtagene autoleucel和 obecabtagene autoleucel(用于成人),在R/R B-ALL中,MRD阴性完全缓解率可达60%-93%。
但问题在于,在部分研究中,未进行移植巩固的患者中,复发率可达68%–100%。
为什么会复发?
CAR-T细胞在体内持续时间不足或白血病细胞通过“丢失”CD19抗原(即抗原逃逸)而躲避免疫攻击。
② 新方向:
靶向CD22 CAR-T和CD19+CD22双靶点CAR-T。
靶向CD22的CAR-T细胞:在CD19靶向治疗后复发的患者中依然有效,完全缓解率达73%-75%,但缓解持续时间较短,可能与癌细胞下调CD22有关。
采用CD19和CD22 CAR-T细胞序贯输注的策略,早期研究显示完全缓解率可达85%以上,12个月无事件生存率在53%–83%之间。但长期疗效仍需随访。
同时靶向CD19和CD22的CAR-T细胞:这是目前的研究热点,旨在从源头上预防或克服单一靶点的抗原逃逸,有多种技术路线(如双特异性CAR、双顺反子CAR、序贯输注等)。
早期临床结果显示完全缓解率同样出色(60%-100%),有望进一步降低复发率。部分研究显示,这种双靶点策略能有效防止CD19阴性复发。
06|未来方向
研究正在探索用免疫治疗替代部分化疗、多种免疫治疗联合、在移植前后应用、新靶点CAR-T(如CD72、TSLPR等)。免疫治疗已成为B-ALL治疗的重要组成部分,而不是“补充选择”。
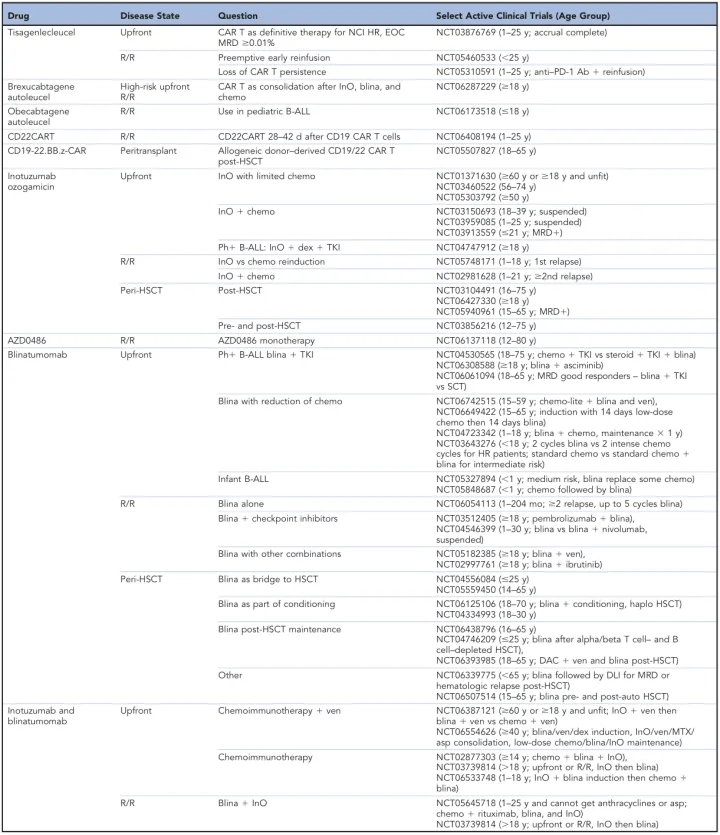
表1 B-ALL免疫治疗中精选的临床试验
对儿童患者来说,B-ALL治愈率已经很高。对成人患者和复发患者来说,免疫治疗正在改变过去的预后。虽然仍然存在复发和副作用挑战,但医学正在持续前进。
未来,B-ALL的治疗可能会更精准、更个体化、更少化疗、更多免疫调控。希望,是建立在科学证据上的。
如果您或家人正在接受B-ALL治疗,建议与您的血液科医生讨论:
是否适合免疫治疗
何时使用
是否需要移植
如何监测副作用
科学正在进步,而您并不孤单。
下面表格是部分白血病临床试验[2],正在各大医院招募受试者,想要了解更多请咨询。

项目 | 靶点 | 适应症 | 要求 |
CC312 | CD19/CD3/CD28的三特异性抗体 | B细胞急性淋巴细胞白血病 | ≥18 岁,复发/难治 |
Senl_B19 | CAR-T疗法 | B细胞急性淋巴细胞白血病 | 3-25 岁,标准治疗失败 |
CAR-T-19 | CAR-T疗法 | 急性B淋巴细胞白血病 | <25,标准治疗失败 |
APG-2575联合阿可替尼 | Bcl-2抑制剂 | 慢性淋巴细胞白血病/小淋巴细胞淋巴瘤 | ≥18,初治 |
ICP-248联合奥布替尼 | Bcl-2抑制剂 | 慢性淋巴细胞白血病/小淋巴细胞淋巴瘤 | 18~80岁,初治 |
LV009 | 体内CAR-T疗法 | B细胞淋巴瘤、白血病 | 18-70 岁,符合复发/难治的标准 |
HMPL-306 | IDH1、IDH2 | 急性髓系白血病 | ≥18 岁,复发/难治 |
XY0206 | FLT3抑制剂 | 急性髓系白血病 | ≥18 岁,标准治疗失败 |
GLB-002 | IKZF1/3 分子胶降解剂 | 急性髓系白血病/骨髓异常综合征 | ≥18 岁,标准治疗失败 |
HMPL-506片 | 伴NPM1突变或/和MLL重排 | 急性髓系白血病(AML)或急性淋巴细胞白血病 | ≥18 岁,复发/难治 |
CG009301 | GSPT1靶向蛋白降解剂 | 急性髓系白血病,急性淋巴白血病、骨髓异常综合征 | 18<75 岁,复发/难治 |
克耐替尼 | EGFR、BTK双靶点靶向药 | 套细胞淋巴瘤、慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL) | ≥18 岁,标准治疗失败 |
凯石招募——临床试验招募平台
参与临床试验的患者,可以免费用试验新药,与试验相关的检查也是免费的。
目前有CAR-T、TIL等细胞疗法,PD-1/PD-L1等免疫治疗药物,小分子抑制剂、双抗、单抗、ADC等靶向药物的临床试验正在进行中。
正在招募肺癌、食管癌、肝癌、胃癌、结直肠癌、宫颈癌、卵巢癌、乳腺癌、胆管癌、子宫内膜癌、黑色素瘤、肉瘤、恶性血液疾病、淋巴瘤等各种恶性肿瘤,想要了解或者参加临床试验项目,可以咨询我们医学部的老师。

参考文献:
1.Davis KL, Yao CC, Zimmerman JAO, et al.Immunotherapy in B-Cell Acute Lymphoblastic Leukemia. J Natl Compr Canc Netw. 2025;23(12):e257067.
2.国家药品监督管理局药品审评中心(CDE)官网.