【招募】卵巢癌进入“基因时代”:我们离更精准的治疗还有多远?
很多患者都会问:“为什么同样是卵巢癌,有的人效果很好,有的人却很快复发?”、“为什么医生一定要我做基因检测?”、“PARP抑制剂到底适不适合我?”。
最新科学综述指出[1]:高级别浆液性卵巢癌(HGSOC)已经全面进入“基因时代”。
我们今天就用通俗的语言,带您深入了解HGSOC的基因组学研究成果,以及这些发现如何转化为更精准的诊断和治疗方法。
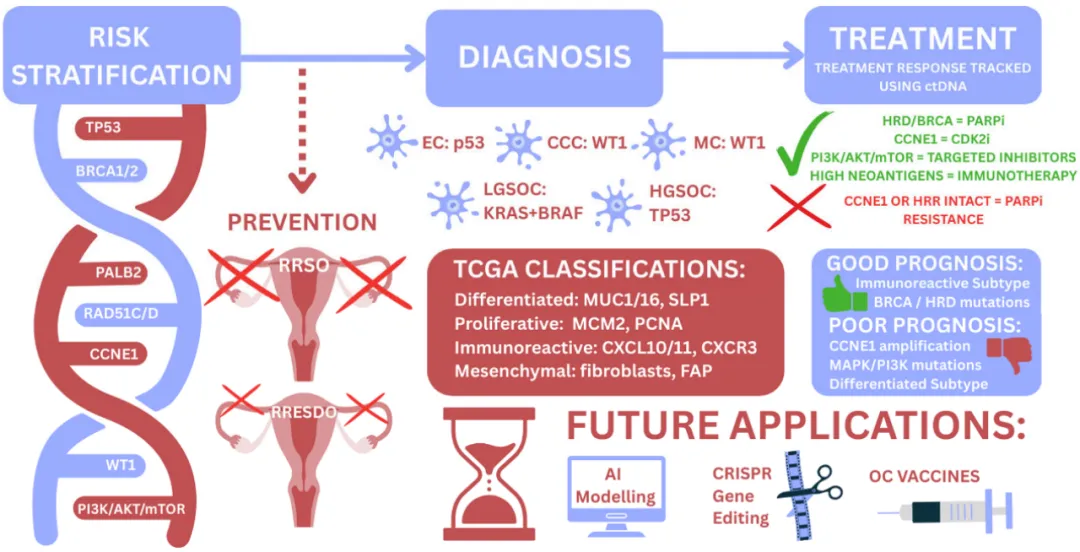
图1 高等级浆液性卵巢癌中基因组学当前应用的图表概要
01|什么是高级别浆液性卵巢癌?
卵巢癌是全球女性面临的严峻健康挑战。2022年,全球约有32.4万名女性被诊断为卵巢癌,超过20.6万人因此失去生命。预计到2050年,这些数字将分别超过50万和35万。其中,HGSOC是最常见也是死亡率最高的一种类型,占卵巢癌死亡的70%以上。
它有几个特点让治疗变得困难,包括:
起病隐匿:早期症状(如腹胀、腹部不适)不典型,约70%的患者确诊时已是晚期。
基因组不稳定:肿瘤细胞的遗传物质充满混乱和错误。
易产生耐药:对初始治疗反应良好,但容易复发并产生耐药。
HGSOC目前5年生存率仅约45%左右,但基因组学的飞速发展正在彻底改变我们对它的认识,并为精准治疗开辟了全新的道路。
02|高级别浆液性卵巢癌的基因组特征:
肿瘤的“身份证”
每个人的肿瘤都有一张独特的“身份证”,而这张身份证就写在它的基因里。理解这些关键基因的改变,是精准治疗的基石。
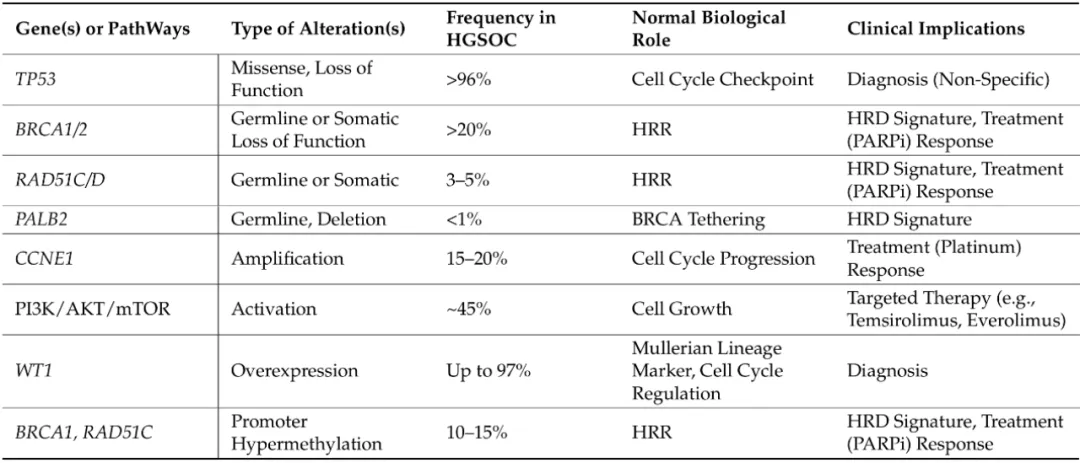
表1 HGSOC中的关键基因组改变及其临床相关性
① TP53突变:几乎普遍存在的变化
研究发现,96%以上的HGSOC存在TP53基因突变。TP53本是一个重要的"抑癌基因",负责阻止异常细胞分裂、修复DNA错误或在细胞无法修复时引导其自我凋亡。
一旦TP53突变,细胞就会失去监管,疯狂增殖,最终形成癌症。但需要注意,尽管TP53突变非常敏感,但并不特异。它可以提示HGSOC,但不能使用它单独确诊。
② BRCA基因:为什么医生一定建议检测?
文献明确指出,超过20%的HGSOC存在BRCA1/2突变(胚系或体细胞)。携带BRCA1突变的女性,一生中患高级别浆液性卵巢癌的风险约为44%,携带BRCA2突变的女性,这一风险约为17%。
BRCA基因负责修复DNA双链断裂和维持基因稳定。当BRCA失效时,细胞无法正确修复DNA,就会形成我们接下来要说的同源重组缺陷(HRD),是目前最重要的治疗突破口。
③ HRD:决定你是否适合PARP抑制剂
同源重组缺陷是此次基因革命中最重要的概念。您可以把它理解为肿瘤细胞的一个致命弱点。
研究发现,大约40–50%的HGSOC存在HRD,除了BRCA1/2,其他相关基因如RAD51C/D、PALB2等的突变也可导致这种缺陷。
HRD阳性的肿瘤对铂类更敏感,对PARP抑制剂反应更好,无进展生存期更长。
目前临床共识认为,根据基因状态不同,PARP抑制剂的获益程度存在明显差异:
BRCA突变型:获益最大。
HRD阳性的BRCA野生型:获益中等。
HRD阴性:获益较小。
需要强调的是,文献也指出,现有的HRD检测方法尚不能完全反映肿瘤实时的DNA修复能力,未来我们需要更精准的“功能性HRD”检测。
④ 其他重要的基因变化
CCNE1扩增:在部分HGSOC中出现,通常意味着肿瘤的DNA修复功能完好(即HRD阴性),常提示对铂类治疗反应较差,预后较差。
PI3K/AKT/mTOR通路异常:这条通路控制细胞的生长和存活,它的异常激活与肿瘤的恶性进展和化疗耐药有关。
03|为什么有的人一开始有效,
后来却耐药?
这正是基因动态变化带来的问题。肿瘤细胞也在“进化”,以逃避药物的追杀。
文献指出了几种耐药机制,包括BRCA“二次修复”突变、BRCA甲基化逆转、DNA修复功能恢复、PI3K/AKT通路激活和复制叉稳定等。
简单理解就是肿瘤会“重新学会”修复DNA,于是对铂类和PARP不再敏感。
因此复发时重新进行基因检测(尤其是通过液体活检动态监测血液中的循环肿瘤DNA)变得越来越重要。
04|基因组学的临床应用:
从诊断到治疗
① 诊断与分型:同样是HGSOC,也分4种类型
基因组学不仅能帮我们确诊,还能对肿瘤进行更精细的分子分型。
根据癌症基因组图谱(TCGA)研究,HGSOC可以分为四种亚型:
免疫反应型:预后最好。
分化型、增殖型、间质型:预后依次变差,对治疗的反应也不同。
这意味着,未来的治疗将不再是“千人一方”,而是基于分子分型的“分型而治”。
② 液体活检:抽血能早期发现卵巢癌?
液体活检是一种通过分析血液中循环肿瘤DNA的非侵入性检测方法。目前研究方向包括ctDNA检测、cfDNA分析和甲基化检测。
它的优势在于微创、可以重复取样、可动态监测肿瘤的变化。
然而,对于早期筛查,但现阶段问题是早期敏感性不足、假阳性率较高等问题,目前尚不能替代传统的影像学和肿瘤标志物(CA-125)检查。
多癌种早期检测试验(如使用循环游离DNA分析)在乳腺癌、肺癌和结直肠癌的早期检测中已显示成功,但对早期HGSOC的敏感性仍有限。
③ 靶向治疗:除了PARP,还有哪些靶向方向?
PARP抑制剂:这是目前最成熟的靶向治疗,如前所述,其疗效高度依赖于HRD状态。
PI3K/AKT/mTOR通路:这一通路异常在HGSOC和透明细胞癌中较为常见(包括PI3CA扩增、AKT激活或PTEN缺失),与不良预后和化疗耐药相关。联合PARP抑制剂是新兴方向,有望克服耐药。
免疫治疗:HRD或高突变负荷肿瘤更易产生新抗原,更容易被免疫系统识别,但目前,免疫检查点抑制剂(如PD-1/PD-L1抑制剂)在卵巢癌中的整体疗效有限,主要在临床试验中探索,或用于罕见的MSI-H/dMMR亚型患者。
抗体偶联药物:Mirvetuximab soravtansine是这方面的代表,能精准识别并杀伤表达叶酸受体α的肿瘤细胞。MIRASOL和PICCOLO试验证实,通过标准化FRα免疫组化进行严格的生物标志物选择,可筛选出从mirvetuximab中获益显著的患者。与化疗相比,改善了耐药患者的生存和患者报告结局。
④ 多组学时代:超越DNA的全面视角
未来趋势是基因组、转录组、蛋白组、代谢组和甲基化多维度整合。例如,研究发现BRCA1基因本身的序列没有突变,但BRCA1启动子甲基化也可造成HRD,KOMET研究提示这类甲基化患者可能对PARP和铂类反应更好。这说明没有突变≠没有功能缺陷。
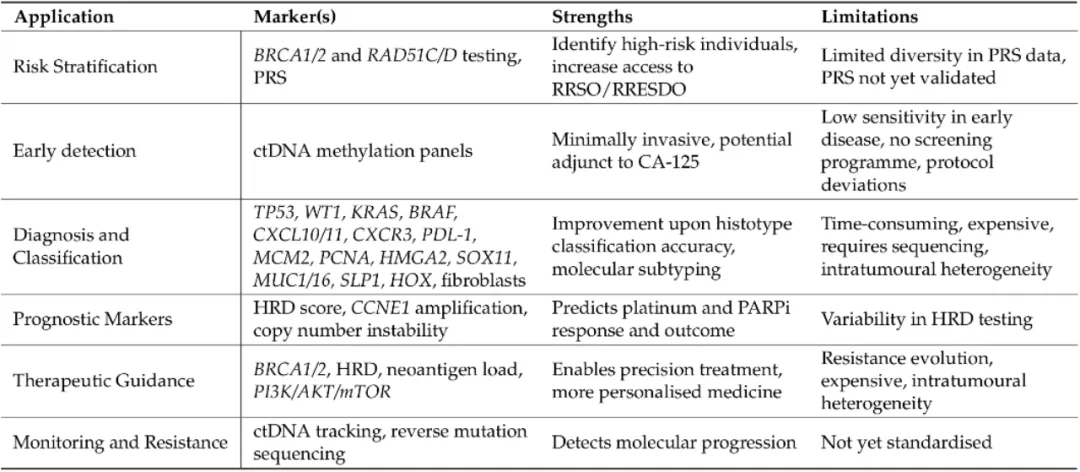
表2 基因组学在高分级浆液性卵巢癌中的临床应用
05|现实挑战与未来希望
尽管前景光明,但前进的道路上仍充满挑战。文献指出了几个关键问题:
肿瘤异质性:同一个肿瘤内,不同区域的基因可能不同,单一部位的穿刺活检可能无法反映全貌。
数据种族偏倚:约80%的基因数据库来自欧洲人群,这意味着研究结果不一定完全适用于其他种族。
成本与可及性:因检测和靶向药物的费用依然高昂。
心理伦理问题:得知携带BRCA突变所带来的焦虑,以及家族成员的风险告知等问题,都需要专业支持。
令人振奋的是,科学家们正在探索更多颠覆性的未来方向:
mRNA卵巢癌疫苗:针对高风险人群,旨在预防高级别浆液性卵巢癌的发生。
CRISPR基因编辑:未来有望直接修复或敲除致病基因。
人工智能:通过深度学习,整合影像、基因组等多维度数据,更精准地预测治疗反应和预后。但需要强调,这些方向目前仍处于研究阶段,尚未成为标准治疗。
06|给患者的现实建议
建议做BRCA检测:这是判断遗传风险和选择靶向药物的基础。
建议进行HRD评估:它能更全面地预测您从PARP抑制剂中的获益程度。
复发时考虑再次基因检测:尤其是通过液体活检,可以帮助揭示耐药机制,指导后续治疗方案。
理解“耐药不是失败,而是生物学变化”。
关注临床试验:如果条件允许,积极了解和参与高质量的临床试验,可能是获得最前沿治疗的重要途径。
如果您正在经历卵巢癌治疗,你并不是在和一个“单一的肿瘤”作战,而是在面对一个不断变化的基因生态系统。但好消息是医学也在进化,精准医学已经开始。
下面表格是部分卵巢癌临床试验[2],正在各大医院招募受试者,想要了解更多请咨询。

项目 | 靶点 | 适应症 | 要求 |
ASN-3186 | BRCA/SMARCA4 | BRCA突变的卵巢癌(包括原发腹膜癌、输卵管癌)、乳腺癌、肺癌 | ≥18岁,至少一线治疗失败 |
DAT-2645 | PARG抑制剂 | 卵巢癌 | ≥18 岁,已知BRCA1/2、HRD阳性的未用过PARP的卵巢癌患者、PARP耐药的卵巢癌患者。 |
XNW29016 | PARG抑制剂 | 卵巢癌、乳腺癌、子宫内膜癌等实体瘤 | ≥18 岁,标准治疗失败 |
SIBP-A19 | ADC药物 | 卵巢癌 | 18~75,标准治疗失败 |
NW-101 | TCR-T疗法 | 卵巢癌 | 18~70,标准治疗失败 |
GC101 | TIL疗法 | 卵巢癌、宫颈癌 | 18~75,一线失败的患者 |
YSCH-01 | 瘤内给药 | 卵巢癌淋巴结转移、肺癌、头颈鳞癌、三阴乳腺癌、脂肪肉瘤 | ≥18 岁,标准治疗失败 |
工程化T细胞疗法 | CAR-T疗法 | 卵巢癌、子宫内膜癌、宫颈癌 | 18-70 岁,标准治疗失败 |
凯石招募——临床试验招募平台
参与临床试验的患者,可以免费用试验新药,与试验相关的检查也是免费的。
目前有CAR-T、TIL等细胞疗法,PD-1/PD-L1等免疫治疗药物,小分子抑制剂、双抗、单抗、ADC等靶向药物的临床试验正在进行中。
正在招募肺癌、食管癌、肝癌、胃癌、结直肠癌、宫颈癌、卵巢癌、乳腺癌、胆管癌、子宫内膜癌、黑色素瘤、肉瘤、恶性血液疾病、淋巴瘤等各种恶性肿瘤,想要了解或者参加临床试验项目,可以咨询我们医学部的老师。

参考文献:
1.Lewis ME, Caricato C, Roberts HL, et al. High-Grade Serous Ovarian Carcinoma in the Genomics Era: Current Applications, Challenges and Future Directions. Int J Mol Sci. 2026;27(3):1617.
2.国家药品监督管理局药品审评中心(CDE)官网.