权威解读:弥漫大B细胞淋巴瘤2026年最新治疗进展
如果你或家人被诊断为弥漫大B细胞淋巴瘤(DLBCL),你可能最关心三个问题:
这是什么病?
还能不能治好?
现在的治疗到底发展到哪一步了?
今天这篇文章,我们基于2026年发布在国际权威血液学期刊上的最新综述[1],为大家梳理当前的治疗格局和未来方向,用患者能听懂的话,帮助您系统梳理:
DLBCL现在怎么治?
不同阶段该如何选择治疗方法?
如果年纪大、身体弱,还有没有治疗机会?
01|什么是弥漫大B细胞淋巴瘤?
DLBCL是最常见的一种非霍奇金淋巴瘤,约占成人淋巴瘤的30%–40%。它的特点可以用一句话概括——进展快,但对治疗反应好,是“可以被治愈”的淋巴瘤。
如果不治疗,病情可能在数周到数月内迅速进展,但如果规范治疗,大多数患者可以获得长期生存,甚至治愈。
数据告诉我们:
在现代治疗条件下,患者总体5年生存率约为65%。
如果患者在完成一线治疗后2年内不复发,其长期生存率可接近普通人群。
02|为什么有的人预后好,
有的人更“难治”?
这是很多患者的疑问,其实DLBCL并不是一种单一疾病。
医生现在主要会从三大方面评估患者风险:
临床因素(传统但仍然重要):
包括年龄、分期(是否为晚期)、体能状态、是否累及多个器官。这些因素组合成一个叫国际预后指数(IPI)的工具,用于判断风险高低。
病理和基因特征(非常关键):
通过病理和基因检测,医生可以识别一些高风险亚型,例如“双打击/三打击”淋巴瘤(某些癌基因同时异常,通常更凶险)、“双表达”淋巴瘤(肿瘤细胞内两种特定蛋白MYC和BCL2高表达,复发风险更高)。
但查出这些亚型并不等于不能治,而是提示需要更密切随访或更先进治疗手段。
治疗过程中的动态评估(未来趋势):
除了PET-CT等影像检查,现在“液体活检”(检测血液中的循环肿瘤DNA,即ctDNA)正展现出巨大潜力。
它不仅具有只需抽血的便利性,并可以比影像提前数月发现复发风险,对判断治疗是否真的清除肿瘤很有价值。这项技术正在逐步走向临床应用。
03|现在DLBCL是怎么治疗的?
与许多需要长期“带瘤生存”的肿瘤不同,DLBCL的治疗目标非常明确:只要条件允许,首选以“治愈”为目的的积极治疗,而不是姑息治疗。
围绕这一目标,治疗方式不断升级,免疫治疗和靶向治疗的加入,使得不同阶段的患者都拥有了比过去更多、也更精准的选择。
① 初治 早期/局限期患者:能少治,就不多治
很多刚确诊的患者最关心的问题是“一定要化疗很多次吗?一定要放疗吗?”。好消息是对于没有高危因素(如大肿块、特定基因异常)的早期(局限期)DLBCL患者,治疗可以“做减法”。
研究已经证实,对于严格筛选的低风险早期患者,仅进行4个周期的免疫化疗(如R-CHOP×4),不联合放疗,其长期疗效与更长疗程或联合放疗相当,但治疗时间更短、副作用更少、生活质量更高。这意味着并不是治得越多越好,而是“恰到好处才是最好的治疗”。
② 初治 进展期/高危患者:在“标准治疗”基础上不断升级
对于分期较晚或具有高危特征的患者,治疗目标同样明确:在不明显增加毒性的前提下,提高治愈率、降低复发风险。
目前的核心策略是在传统标准化疗(如R-CHOP)基础上引入新药。其中最重要的进展之一是Polatuzumab(维泊妥珠单抗,是一种抗体药物偶联物)+R-CHP(Pola-R-CHP)。
研究显示,与传统R-CHOP相比,该方案可延长无进展生存期,且副作用总体可控,已成为部分中高危患者重要的一线治疗选择之一。这些进展说明,即使是“高危”患者,治疗方案也在不断升级,而不是停滞不前。
③ 复发/难治患者:选择比过去多得多
这可能是患者最恐惧的问题,但2026年面对复发/难治的DLBCL,治疗格局已经和10年前截然不同。
目前的重要手段包括:
CAR-T细胞治疗:
该方法通过提取患者自身的免疫T细胞,使其成为精准杀伤肿瘤的“特种兵”。对一线治疗后12个月内复发或原发耐药的患者疗效显著,抗CD19 CAR-T已成为二线治疗的“金标准”,疗效明确优于传统的化疗+自体干细胞移植。
双特异性抗体:
该方法不需要细胞回输,可反复使用,可及性高,对不能做移植或CAR-T的患者尤其重要。
单药治疗方案:
Epcoritamab和Glofitamab(格菲妥单抗)等药物已获批用于三线及以上治疗。即使经过多线治疗,仍有约40%的患者能达到完全缓解,且缓解可能非常持久。
联合治疗方案:
双特异性抗体与化疗或抗体药物偶联物(ADC)联用疗效更佳。例如Mosunetuzumab(莫妥珠单抗)联合Polatuzumab(维泊妥珠单抗)的方案,疗效已被证明优于传统化疗,成为复发/难治患者新的重要选择之一。
抗体偶联药物(ADC):
该方案能将高活性的化疗药精准投送至肿瘤细胞,减少对正常组织的伤害,副作用相对传统化疗更可控。
这些治疗正在逐步减少对传统化疗的依赖,让治疗更精准、更人性化。
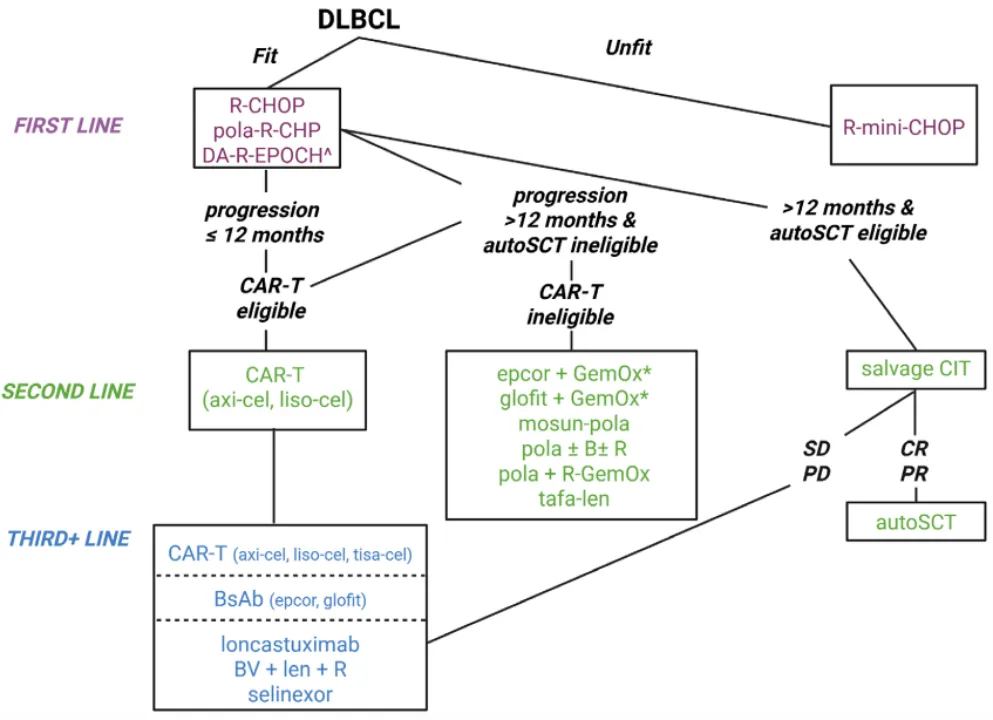
图1 DLBCL 治疗决策路径图
04|如果年纪大、身体弱怎么办?
很多患者和家属会担心“年纪大了、身体差,是不是就没办法治了?”。答案是:不是。
现代治疗策略正在变得更加个体化:
① 减量化疗方案,例如R-miniCHOP:
在科学降低化疗剂量的同时尽量保留疗效,显著降低了毒性和治疗风险,这是目前老年患者中非常重要、成熟的方案。
② 无化疗方案:这是当前研究的热点。
研究发现,完全不含传统化疗的药物组合也能有效控制DLBCL。
例如,固定疗程的双特异性抗体单药治疗(如Mosunetuzumab、Epcoritamab),在大量不适合化疗的老年或体弱患者中,已经显示出客观的疗效和可控的安全性。这为很多“原本没有好选择”的患者,提供了真正有分量的新出路。
总的来说,DLBCL的治疗,首先要看“病到什么程度”(分期与风险),再看“身体能不能承受”(体能状态与合并症),而不是简单地按年龄或一次治疗失败下结论。
05|对患者来说,最重要的几句话
你需要记住这些:
① DLBCL是一种高度可治愈的恶性肿瘤。
② 治疗方案越来越个体化,不是“一个方案走到底”。
③ 即使复发,也不等于没有办法。
④ 规范治疗和定期随访非常关键。
⑤ 不要自行放弃或延误治疗时机。
如果你正在经历焦虑、恐惧、反复查资料的阶段,请相信,这不是你的问题,而是任何一个面对“癌”字的人都会有的反应。
但我们想告诉你一句最朴素的结论:DLBCL,是目前淋巴瘤治疗中,治疗方案进展最快、最有希望“攻克”的类型之一。
下面表格是部分淋巴瘤临床试验[2],正在各大医院招募受试者,想要了解更多请咨询。

项目 | 靶点 | 适应症 | 要求 |
B019注射液 | CAR-T疗法 | 弥漫大B非霍奇金淋巴瘤 | 18-70 岁,标准治疗失败 |
BEBT-908 联合利妥昔单抗 | 双靶点抑制剂 | 弥漫大B细胞淋巴瘤 | 18~75,标准治疗失败 |
迪诺仑赛注射液 | CAR-T疗法 | 弥漫大B淋巴瘤 | ≥18岁,至少二线治疗后 |
GLB-002 | IKZF1/3 分子胶降解剂 | 非霍奇金淋巴瘤 | ≥18 岁,标准治疗失败 |
RJMty19 | 通用型CD19-CAR-DNT | 非霍奇金淋巴瘤 | 18~65,标准治疗失败 |
SepantroniumBromide(PC-002)联合利妥昔单抗 | DUB抑制剂 | 伯基特淋巴瘤+弥漫大B | ≥18岁,标准治疗失败 |
LV009 | 体内CAR-T疗法 | B细胞淋巴瘤、白血病 | 18-70 岁,符合复发/难治的标准 |
PA3-17 | CAR-T疗法 | CD7阳性的T急淋和T淋母 | 18-70 岁,标准治疗失败 |
XNW5004 | EZH2抑制剂 | 外周T细胞淋巴瘤 | 18~70岁,接受过至少一种系统治疗 |
IM19 CAR-T | CAR-T疗法 | 套细胞淋巴瘤 | ≥18岁,至少二线失败 |
奥布替尼+苯达莫司汀+利妥昔 | BTK抑制剂 | 套细胞淋巴瘤 | ≥60岁,初治 |
克耐替尼 | EGFR、BTK双靶点靶向药 | 套细胞淋巴瘤、慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL) | ≥18 岁,标准治疗失败 |
APG-2575联合阿可替尼 | Bcl-2抑制剂 | 慢性淋巴细胞白血病/小淋巴细胞淋巴瘤 | ≥18,初治 |
ICP-248联合奥布替尼 | Bcl-2抑制剂 | 慢性淋巴细胞白血病/小淋巴细胞淋巴瘤 | 18~80岁,初治 |
LV009 | 体内CAR-T疗法 | B细胞淋巴瘤、白血病 | 18-70 岁,符合复发/难治的标准 |
凯石招募——临床试验招募平台
参与临床试验的患者,可以免费用试验新药,与试验相关的检查也是免费的。
目前有CAR-T、TIL等细胞疗法,PD-1/PD-L1等免疫治疗药物,小分子抑制剂、双抗、单抗、ADC等靶向药物的临床试验正在进行中。
正在招募肺癌、食管癌、肝癌、胃癌、结直肠癌、宫颈癌、卵巢癌、乳腺癌、胆管癌、子宫内膜癌、黑色素瘤、肉瘤、恶性血液疾病、淋巴瘤等各种恶性肿瘤,想要了解或者参加临床试验项目,可以咨询我们医学部的老师。

参考文献:
1.Chong EA, Tomasulo EB, Barta SK. et al.2026 Update on the Management of Diffuse Large B-Cell Lymphoma. Am J Hematol. Published online February 7, 2026.
2.国家药品监督管理局药品审评中心(CDE)官网.