肺癌真实世界研究,H药斯鲁利单抗一线治疗晚期鳞状非小细胞肺癌,疾病控制率100%,ORR为58.70%,验证了在肺癌临床价值
H药 汉斯状®(通用名:斯鲁利单抗注射液)是上海复宏汉霖公司自主研发的创新型重组人源化抗PD-1单抗注射液[1]。
在2024年12月3日,汉斯状®获得国家药品监督管理局批准,联合培美曲塞和卡铂适用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌(nsq-NSCLC)的一线治疗[1]。
在2022年11月1日,汉斯状®已经在国内获批,联合卡铂和白蛋白紫杉醇用于一线治疗不可手术切除的局部晚期或转移性鳞状非小细胞肺癌(sq-NSCLC)[2]。


1、斯鲁利单抗一线治疗晚期鳞状非小细胞肺癌(sq-NSCLC)的真实世界研究[4]
该研究纳入了经病理或细胞学检查确诊为晚期鳞状非小细胞肺癌,且不适合手术或放疗的患者。这些患者在2022年至2024年间,接受了斯鲁利单抗一线治疗。所有患者均完成了至少两个疗程的斯鲁利单抗治疗。
共纳入46例晚期sqNSCLC患者,其中27例为III期,19例为IV期。中位年龄为67岁(范围:41-86岁),中位随访时间为12个月(范围:1.47-24.63个月)。
21例患者(21/46,45.65%)出现疾病进展,中位无进展生存期(PFS)为11.0个月。6个月和1年的无进展生存率(PFS)分别为78.14%和48.21%,亚组分析未发现影响PFS的统计学显著因素。
在接受治疗的患者中,27 例达到部分缓解 (PR),客观缓解率(ORR)为58.70%。疾病控制率(DCR)为100%,1 年总生存率 (OS) 为 85.21%。
结论:在这项真实世界的研究中,斯鲁利单抗表现出显著的疗效和良好的耐受性安全性,支持将其用作晚期鳞状非小细胞肺癌的一线高效免疫疗法治疗选择。
2、斯鲁利单抗新辅助治疗局部晚期驱动基因阴性非小细胞肺癌的疗效和安全性:一项多中心真实世界研究[5]
该研究纳入了经组织学确诊的局部晚期非小细胞肺癌患者,且这些患者无可靶向的基因组改变。患者接受了至少 1 个周期的斯鲁利单抗(300 毫克,每 3 周一次)联合铂类化疗的新辅助治疗,随后进行了根治性手术。
2022年1月至2024年12月期间,共纳入27例患者(中位年龄64岁),其中81.5%(22/27)患者处在III期。在这些患者中,92.6%(25/27)实现了 R0 切除。
病理评估显示,主要病理缓解(MPR)率为74.1%(20/27),病理完全缓解(pCR)率为33.3%(9/27)。影像学检查显示,有2例完全缓解(CR)和20例部分缓解(PR),客观缓解率(ORR)为81.5%(22/27),疾病控制率(DCR)为96.3%(26/27)。
目前国内有斯鲁利单抗相关的肺癌临床试验进行中,招募患者免费参加。

在2025年世界肺癌大会(WCLC)上,复宏汉霖公布了PD-L1靶向抗体偶联药物(ADC)HLX43治疗晚期/转移性实体瘤的I期临床数据[7]。
这次公布的主要是非小细胞肺癌(NSCLC)患者研究数据,截至2025年6月28日,共入组了56例NSCLC患者(Ia期+Ib期2.0 mg/kg剂量组及2.5 mg/kg剂量组),其中29例(51.8%)为鳞癌患者,27例(48.2%)为非鳞癌患者,这些患者接受过铂类药物治疗或免疫治疗或靶向治疗。
在54例可评估患者中,整体客观缓解率(ORR)为37.0%,疾病控制率(DCR)为87.0%。在26例接受过3线及以上治疗的非鳞癌患者中,ORR为46.2%,DCR为96.2%;在28例接受过4线及以上治疗的鳞癌患者中,ORR为28.6%,DCR为82.1%。
亚组分析显示,在EGFR野生型的非鳞NSCLC患者(n=15)中,经确认的客观缓解率(cORR)为46.7%,DCR为93.3%,在PD-L1阴性(TPS<1%,n=21)人群的ORR为38.1%,DCR为85.7%,提示HLX43的抗肿瘤活性并不依赖于PD-L1表达水平。
参与临床试验的患者,可以免费用试验新药,与试验相关的检查也是免费的。
目前有CAR-T、TIL等细胞疗法,PD-1/PD-L1等免疫治疗药物,小分子抑制剂、双抗、单抗、ADC等靶向药物的临床试验正在进行中。
正在招募肺癌、食管癌、肝癌、胃癌、结直肠癌、宫颈癌、卵巢癌、乳腺癌、胆管癌、子宫内膜癌、黑色素瘤、肉瘤、恶性血液疾病、淋巴瘤等各种恶性肿瘤,想要了解或者参加临床试验项目,可以咨询我们医学部的老师。

参考文献:
1.再迎突破!复宏汉霖H药 汉斯状®获批非鳞状非小细胞肺癌新适应症,复宏汉霖微信公众号,文章发布于2024年12月3日.
2.再下一城!复宏汉霖创新抗PD-1单抗H药 汉斯状®获批治疗鳞状非小细胞肺癌,复宏汉霖微信公众号,文章发布于2022年11月1日.
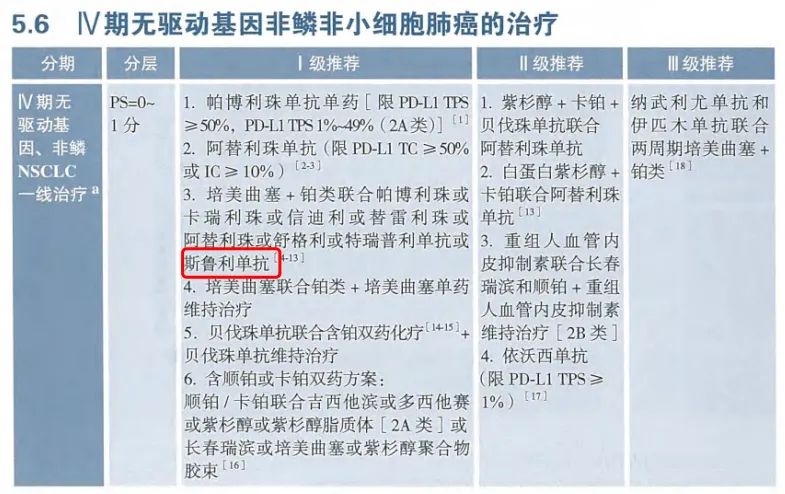
3.2025年中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南.
4. J. Zhou, M. Wan, M. Zhong,et al. Real-world study of serplulimab as first-line treatment for advanced squamous non-small-cell lung cancer.[J].2025 ESMO ASIA.
5. N. Lin, Z. Yang, J. Lin,et al. Efficacy and safety of neoadjuvant serplulimab in locally advanced driver gene-negative NSCLC: A multicenter real-world study.[J].2025 ESMO ASIA.
6.国家药品监督管理局药品审评中心(CDE)官网.
7.WCLC 专家说 | 王洁教授:HLX43广谱抗肿瘤潜力凸显,PD-L1 ADC开启实体瘤治疗新篇章,复宏汉霖微信公众号,文章发布于2025年9月11日.