BRCA1突变不再是“诅咒”,而是抗癌“加速器”!卵巢癌患者的未来治疗蓝图
从“遗传风险”到“治疗优势”——你手握的基因“王牌”!
确诊BRCA1基因突变相关的卵巢癌,许多患者的第一反应是担忧遗传和高风险。然而,在肿瘤医学界,BRCA1突变已经被公认为一种独特的“基因优势”!这一突变暴露了肿瘤细胞在DNA修复机制上的致命弱点,使癌细胞对特定药物(特别是PARP抑制剂和铂类化疗)高度敏感。
本文将为您梳理卵巢癌治疗领域的最新进展,为您揭示如何利用您的BRCA1 “王牌”,从目前的“黄金标准”迈向未来的“进阶疗法”。
一、您的“基因身份证”——为什么BRCA1如此特殊?
1. BRCA1的本职工作:修复DNA双链
细胞的DNA经常会出现损伤,其中最危险的一种叫双链断裂(DSB),就是把DNA的两股链都“剪断”,如果修不好,细胞就会死亡。
修复DSB有两条主要路径(如表格所示):
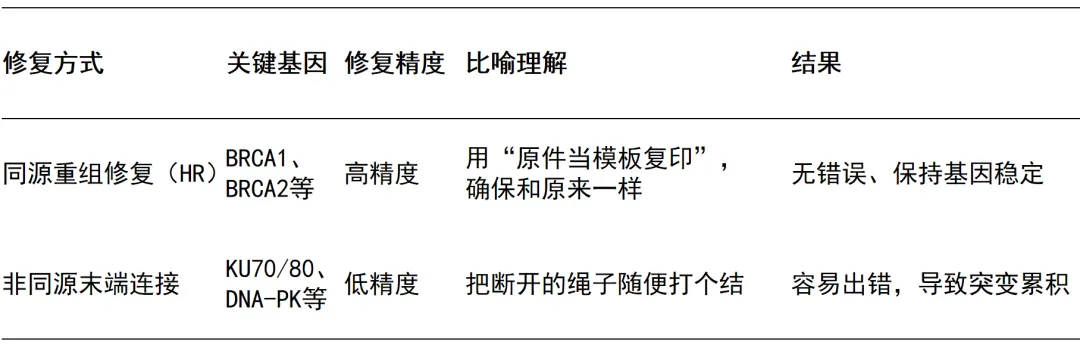
正常细胞能用BRCA1参与的HR修复DNA,从而使细胞更稳定。如果BRCA1突变/缺失,高精度的HR修复无法进行,细胞失去“修复双链断裂的黄金方案”,就会导致DNA损伤不断累积、细胞压力变大、难以生存。
这些BRCA1缺陷的肿瘤细胞为了存活,它们会改走备用路径:PARP(尤其是PARP1)主要负责处理的单链断裂修复(SSB),单链断裂不及时修好,会在DNA复制时变成DSB。但此时BRCA1已经坏了,不能修复DSB(如下图所示[1])。
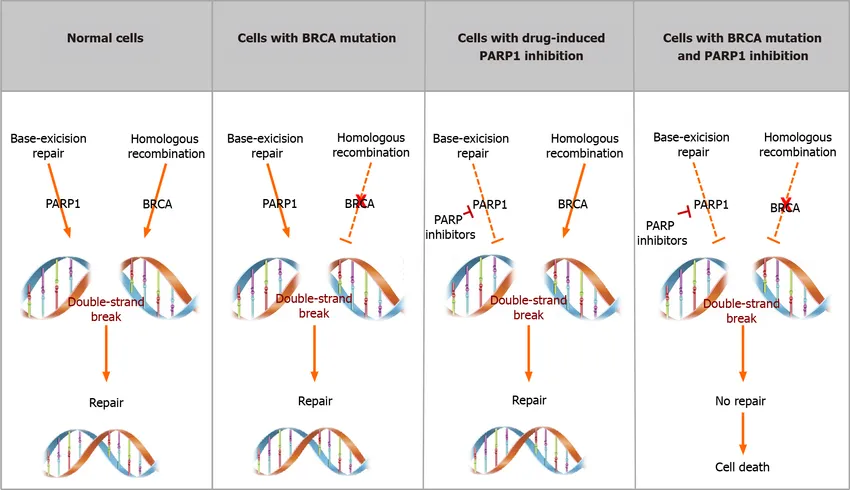
(BRCA、PARP抑制剂的合成致死性)
也就是说:
1、BRCA1缺陷肿瘤靠PARP来“托住生命线”。
2、PARP负责帮忙避免双链断裂的发生。
3、一旦PARP也被抑制,细胞就无法维持DNA完整性,细胞就会死亡。
因此BRCA1突变的肿瘤对PARP抑制剂非常敏感,它是BRCA1突变患者的独有治疗机遇。
二、【历史性里程碑】PARP抑制剂
将BRCA1突变劣势,彻底转化为“治疗优势”的划时代药物!
PARP抑制剂是BRCA1突变卵巢癌治疗的基石,无论是作为一线巩固还是复发维持治疗,都显示出卓越的疗效。
目前常用药物
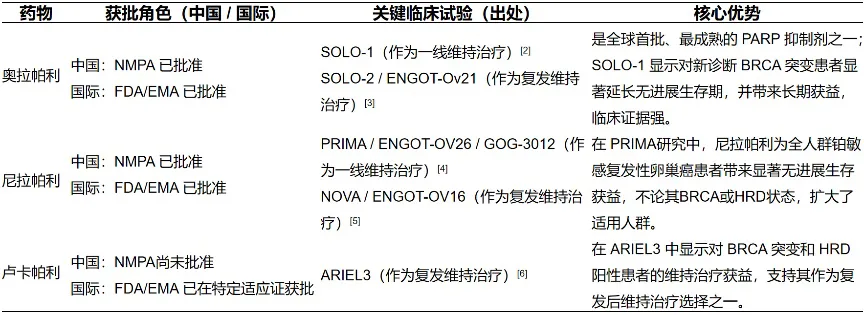
大量循证证据表明,PARP抑制剂在BRCA1基因突变型卵巢癌的治疗中,展现出卓越的疗效与良好的耐受性。
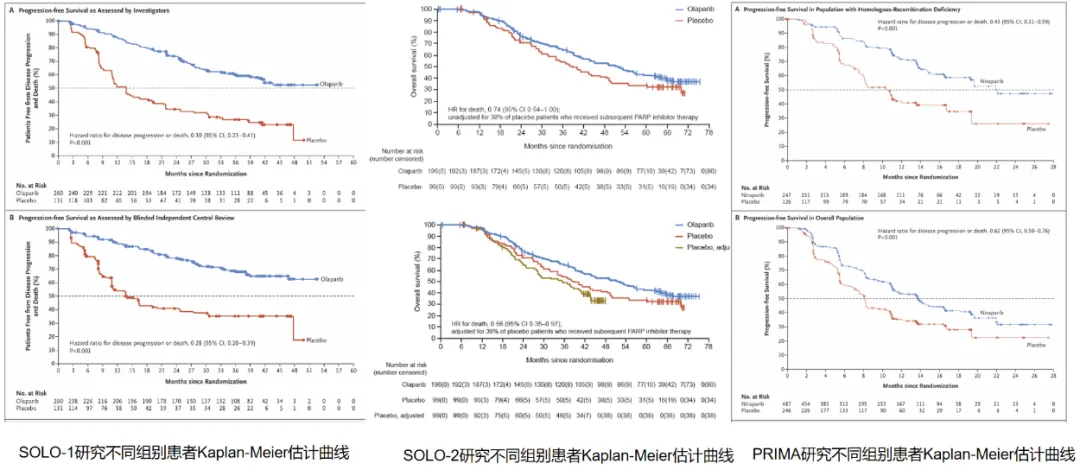
❶发表在《新英格兰》的一项国际大型临床试验(SOLO1)表明,对于携带BRCA基因突变、且化疗后病情控制的新诊断晚期卵巢癌患者,在接受约2年的奥拉帕利维持治疗后,其3年无进展生存率提升至60%(安慰剂组为27%),疾病进展或死亡风险显著降低70%,中位无进展生存期延长约3年。
❷发表在《柳叶刀》上的SOLO2/ENGOT-Ov21研究是首个在BRCA突变铂敏感复发性卵巢癌群体中证实PARP抑制剂维持治疗能带来明确总生存获益的III期研究,其结果表明,对携带BRCA突变、对铂类药物敏感的复发性卵巢癌患者(曾接受过至少两线铂类化疗),与安慰剂相比,使用奥拉帕利(300mg,每日两次)作为维持治疗,能够显著延长患者的总生存期,中位总生存期延长了12.9个月(51.7个月 vs 38.8个月)。
❸发表于《新英格兰》的PRIMA/ENGOT-OV26/GOG-3012 III期随机双盲试验结果显示,在具有同源重组缺陷的患者中,尼拉帕利组的中位无进展生存期显著优于安慰剂组(21.9个月vs 10.4个月),在总体人群中也显著延长无进展生存期(13.8个月vs 8.2个月)。24个月时的中期总生存率在尼拉帕利组为84%,安慰剂组为77%。该研究首次证实尼拉帕利作为一线维持治疗可为全人群晚期卵巢癌患者带来显著无进展生存获益,无论其同源重组状态如何。
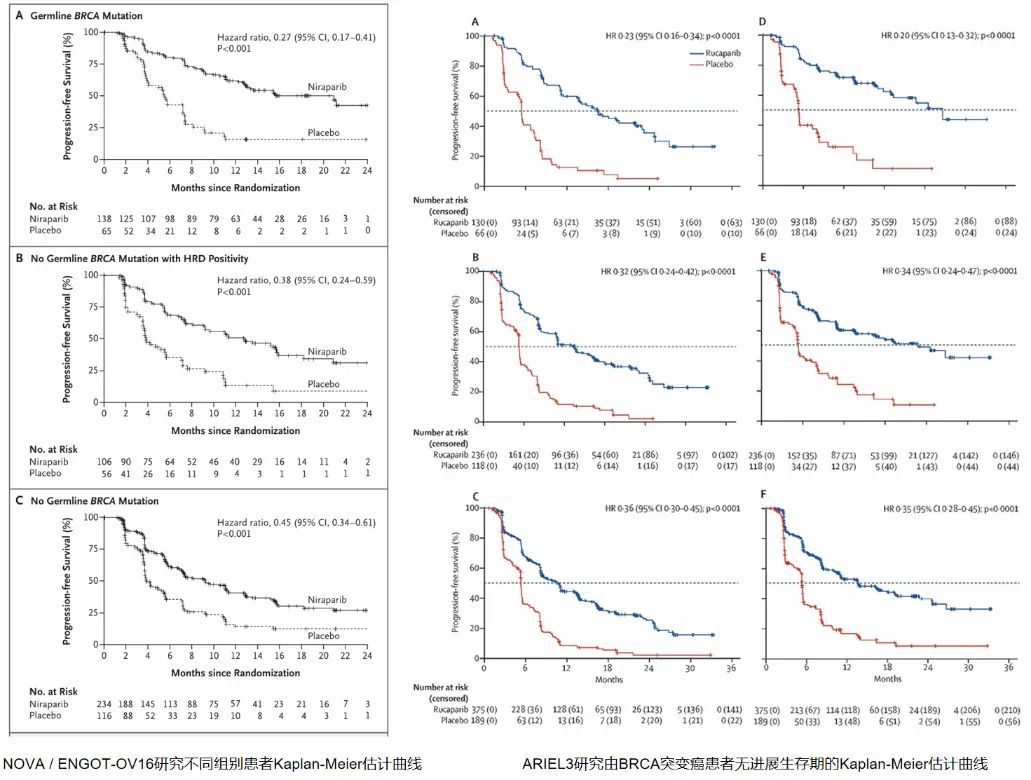
❹发表于《新英格兰》的ENGOT-OV16/NOVA III期随机双盲试验纳入553名对最近一次铂类化疗有应答(完全或部分缓解)且无铂间期超过6个月的复发性卵巢癌患者,按是否存在胚系BRCA突变(gBRCA队列和非gBRCA队列)分层,并以2:1比例随机分配至尼拉帕利组(300 mg,每日一次)或安慰剂组,持续治疗直至疾病进展。结果显示,在gBRCA突变队列中,尼拉帕利组中位无进展生存期显著优于安慰剂组(21.0个月 vs 5.5个月);在非gBRCA队列中,无论其肿瘤是否存在同源重组缺陷,尼拉帕利均显著延长无进展生存期(HRD阳性亚组:12.9个月 vs 3.8个月;总体非gBRCA队列:9.3个月 vs 3.9个月)。
❺发表在《柳叶刀》的ARIEL3 III期随机双盲试验纳入564名对最近一次铂类化疗(至少接受过两线含铂方案)达到完全或部分缓解的高级别浆液性或子宫内膜样卵巢癌、原发性腹膜癌或输卵管癌患者,按2:1比例随机分配至卢卡帕利组(600 mg,每日两次)或安慰剂组。结果表明,在BRCA突变患者中,卢卡帕利组中位无进展生存期显著优于安慰剂组(16.6个月 vs 5.4个月)。
尽管PARP抑制剂已在BRCA突变卵巢癌的治疗中树立起一座丰碑,但科学的探索步伐从未停歇。当前的研究前沿,正从巩固疗效走向开拓新的疆域。
三、前沿进展:最新研究方向快照
1、新一代PARP1选择性抑制剂AZD5305
尽管PARPi已广泛应用于BRCA1/2突变相关的卵巢癌。然而,第一代PARP1/2抑制剂(如奥拉帕利)存在血液学毒性,且易产生耐药。AZD5305是高选择性PARP1抑制剂,旨在提高疗效并改善安全性。
2024年一项临床前研究[7]利用13例来源于患者的肿瘤异种移植模型,系统评估了AZD5305单药及联合化疗/ATR抑制剂的疗效,结果表明,AZD5305单药疗效显著优于奥拉帕利:完全缓解率(pCRR)达75% vs 37%,中位无进展生存期(pPFS)>386天 vs 90天。
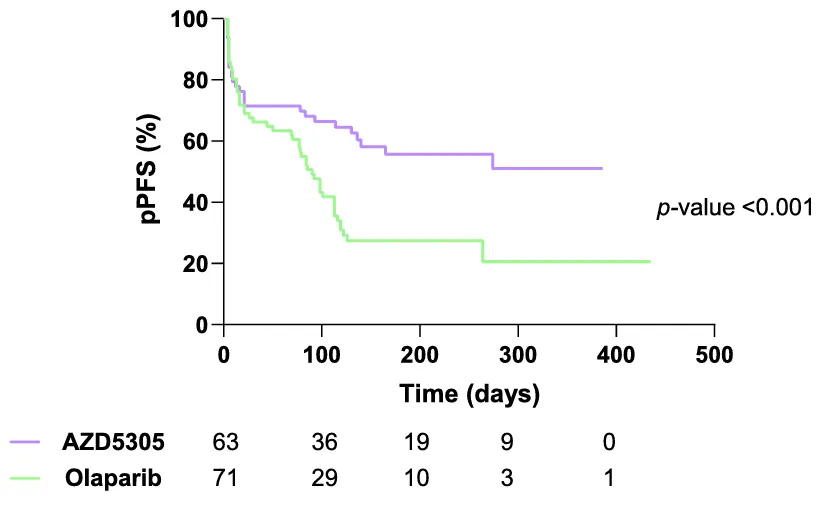
(AZD5305和奥拉帕利治疗的个体肿瘤的无进展生存率)
进一步研究还发现,AZD5305联合治疗策略能够有效克服耐药:AZD5305联合卡铂在3/6模型中诱导深度缓解,AZD5305联合ATR抑制剂(ceralasertib)在5/5模型中实现持续缓解。
AZD5305作为新一代PARP1选择性抑制剂,不仅在单药治疗中表现出更强效和持久的抗肿瘤活性,还具备与化疗或ATR抑制剂联合应用的潜力,为HR缺陷型肿瘤患者提供了新的治疗选择。
NCT04644068是第一项使用AZD5305的I/IIa期临床研究,旨在评估递增剂量的AZD5305 作为单一疗法和与抗癌药物联合治疗晚期实体恶性肿瘤患者(包括卵巢癌)的安全性、耐受性、药代动力学、药效学和初步疗效。
在2024年American Association for Cancer Research (AACR) 年会上,发表了Ⅰ/Ⅱa期的结果摘要:在使用 AZD5305 60 mg每日剂量的队列(n≈31)中,客观缓解率(ORR)为约48.4%,中位缓解持续时间为7.3个月,中位无进展生存期为约9.1个月。同时,安全性良好:与第一代 PARP抑制剂相比,血液学毒性和剂量中断率更低。该试验目前仍在进行中,成果令人期待。
2、应对PARP抑制剂耐药 — Polθ抑制剂[8]
尽管PARP抑制剂为BRCA1/2突变等同源重组修复缺陷肿瘤带来革命性疗法,但约40-70%患者出现先天或获得性耐药,亟需新策略克服这一缺陷。
新星靶点:Polθ
Polθ由POLQ基因编码,抑制BRCA缺陷肿瘤依赖的替代DNA修复路径,可在PARP抑制剂耐药时再次杀伤肿瘤。
研究发现:
1、Polθ与HR基因存在合成致死关系:在BRCA1/2缺陷细胞中,抑制Polθ导致细胞死亡。
2、Polθ高表达于多种癌症,与预后不良、放疗化疗抵抗相关。
3、抑制Polθ可逆转PARP抑制剂耐药,尤其对存在BRCA回复突变的肿瘤有效。
目前,多项I/II期临床试验正在进行中,探索Polθ抑制剂单药或与PARP抑制剂联用,比如NCT04991480、NCT05898399、NCT05687110。
Polθ作为新兴合成致死靶点,不仅有望解决PARP抑制剂耐药难题,还拓展了与放疗、免疫治疗的联合空间。随着临床数据的积累,Polθ抑制剂有望成为BRCA1基因突变相关的卵巢癌治疗的重要新武器。
3、联合治疗策略——ATR抑制剂+PARPi[9]
铂耐药复发的高级别浆液性卵巢癌(HGSOC)治疗选择有限,预后极差。PARP抑制剂在HR缺陷患者中有效,但在铂耐药且未经选择的患者中反应率低。
但一项名为 CAPRI 的II期临床试验首次证实:在对PARP抑制剂产生获得性耐药的铂敏感、同源重组缺陷的HGSOC患者中,ATR抑制剂ceralasertib联合PARP抑制剂olaparib,仍能带来50%的客观缓解率(ORR),且安全性可控。
研究设计
患者群体:13例铂敏感、同源重组缺陷或BRCA突变的复发HGSOC患者,均在既往PARP抑制剂治疗中获益,之后出现进展。
治疗方案:olaparib 300mg 每日两次 + ceralasertib 160mg 每日一次(第1–7天),28天为一周期。
研究结果
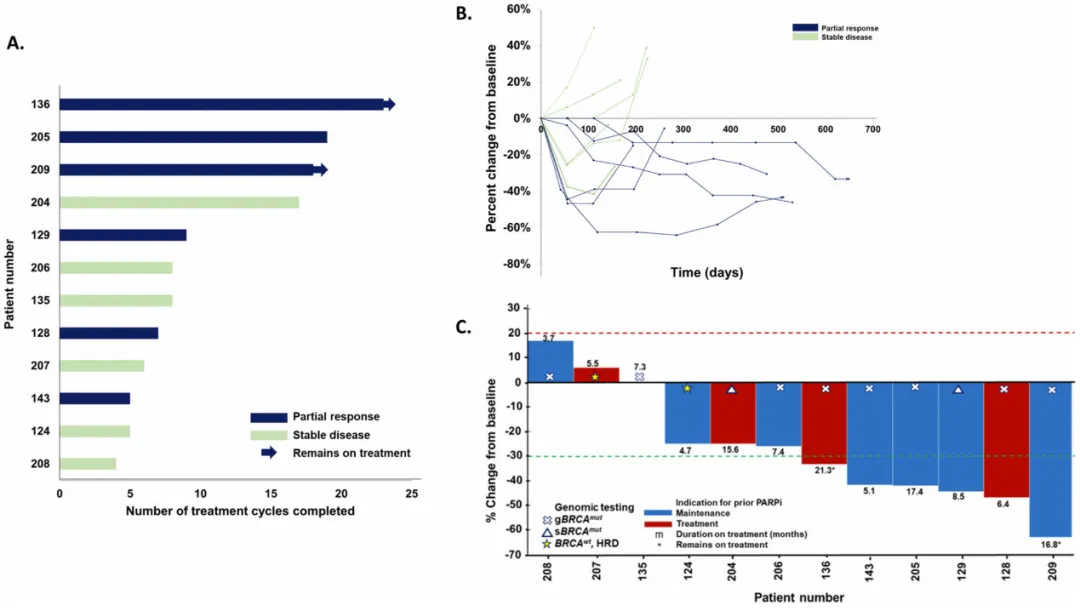
(奥拉帕利和赛拉塞替尼的反应和持续时间)
疗效显著
ORR为50%(6/12例患者达到部分缓解,PR)
中位PFS为7.43个月
86%的患者CA-125下降超过50%
多数患者在治疗3个周期内即出现最佳反应
安全性良好
G3/4级不良事件发生率为38%,主要为血液学毒性(贫血、血小板减少、中性粒细胞减少)
无患者因毒性停药
4例患者需剂量调整,整体耐受性良好
该研究首次在获得性PARP抑制剂耐药人群中证实了ATR抑制剂联合PARP抑制剂(CAPRI方案)具有显著抗肿瘤活性。该联合方案相比现有后线治疗(如化疗或WEE1抑制剂联合方案)展现出更优疗效与更低毒性,为耐药患者提供了一种免化疗的靶向治疗新选择。
4、免疫治疗+PARPi[10]
为了应对PARP抑制剂的耐药问题,研究者们开展了MEDIOLA II期研究,该研究根据gBRCA突变状态和用药方案将患者分为三个队列:gBRCA突变患者接受奥拉帕利联合度伐利尤单抗双药治疗;非gBRCA突变患者则进一步分为双药治疗组(奥拉帕利+度伐利尤单抗)和三药治疗组(奥拉帕利+度伐利尤单抗+贝伐珠单抗)。
研究结果:gBRCAm扩展双药组疗效卓越(ORR 92.2%,中位PFS 15.0个月),非gBRCAm三药组疗效同样突出(ORR 87.1%,中位PFS 14.7个月,中位OS 31.9个月),而非gBRCAm双药组疗效相对有限(24周DCR 28.1%),提示在非gBRCA突变人群中双药方案疗效不足,需联合贝伐珠单抗以提升疗效。
安全性分析:安全性特征与各单药已知安全性一致,未发现新的安全信号;最常见≥3级不良事件为贫血;三药组因不良事件导致任何治疗终止的比例较高(32.3%),主要与贝伐珠单抗相关。
MEDIOLA研究结果表明,Olaparib + Durvalumab在gBRCAm PSROC中疗效卓越,而加入Bevacizumab的三联方案在非gBRCAm PSROC中同样表现出高疗效且安全性可控,为不同基因背景的复发卵巢癌患者提供了新的“免化疗”治疗选择。
5、靶向抗体-药物偶联(ADC)[11]
美国食品药品监督管理局(FDA)已于2022年11月14日加速批准了抗体偶联药物Mirvetuximab soravtansine-gynx(索米妥昔单抗),这是首个针对铂耐药卵巢癌的生物标志物导向疗法,标志着该领域治疗模式的重大转变。
药物机制:精准打击肿瘤细胞
索米妥昔单抗是一种抗体药物偶联物,由以下三部分构成:
1、人源化抗FRα单抗:特异性结合肿瘤细胞表面的叶酸受体α;
2、可裂解连接子:在细胞内释放有效载荷;
3、细胞毒性分子DM4:抑制微管聚合,诱导细胞凋亡。
其独特之处在于具备 “旁观者效应” :DM4代谢物可扩散至邻近FRα阴性肿瘤细胞,扩大杀伤范围。
索米妥昔单抗相关的关键临床试验概览

索米妥昔单抗的毒性主要为低级别眼部和胃肠道反应,其中眼部毒性管理是治疗过程中的重点。
四、作为患者,我们可以做什么
1.确认基因检测:明确BRCA1状态。
2.整理既往治疗史:PARPi 用药史、铂类敏感性、影像与标志物。
3.咨询医生/临床试验协调员:确认是否符合试验入组条件。
4.关注副作用与生活质量:了解血液学、消化道等潜在毒性。
5.加入凯石招募:获取试验信息与病友经验。
BRCA1 突变曾是坏消息,但也提供了精准治疗的“钥匙”。从PARP抑制剂到Polθ抑制剂、联合策略,再到ADC与免疫组合,科学在不断为患者开辟新路径。建议基因检测、关注临床试验,与医生讨论最适合你的治疗方案。
现有多项卵巢癌临床试验正在各大医院招募肿瘤患者,欢迎咨询!

项目 | 靶点 | 适应症 | 要求 |
ASN-3186 | BRCA/SMARCA4 | BRCA突变的卵巢癌(包括原发腹膜癌、输卵管癌)、乳腺癌、肺癌 | ≥18岁,至少一线治疗失败 |
DAT-2645 | PARG抑制剂 | 卵巢癌 | ≥18 岁,已知BRCA1/2、HRD阳性的未用过PARP的卵巢癌患者、PARP耐药的卵巢癌患者。 |
NW-101 | TCR-T疗法 | 卵巢癌 | 18~70,标准治疗失败 |
SIBP-A19 | ADC药物 | 卵巢癌 | 18~75,标准治疗失败 |
MSLN-CAR-T | CAR-T疗法 | 卵巢癌、间皮瘤 | 18~70岁,二线治疗失败的患者 |
GC101 | TIL疗法 | 卵巢癌、宫颈癌 | 18~75,一线失败的患者 |
YSCH-01 | 瘤内给药 | 卵巢癌淋巴结转移、肺癌、头颈鳞癌、三阴乳腺瘟、脂肪肉瘤 | ≥18 岁,标准治疗失败 |
工程化T细胞疗法 | CAR-T疗法 | 卵巢癌、子宫内膜癌、宫颈癌 | 18-70 岁,标准治疗失败 |
XNW29016 | PARG抑制剂 | 卵巢癌、乳腺癌、子宫内膜癌等实体瘤 | ≥18 岁,标准治疗失败 |
凯石招募——临床试验招募平台
参与临床试验的患者,可以免费用试验新药,与试验相关的检查也是免费的。
目前有CAR-T、TIL等细胞疗法,PD-1/PD-L1等免疫治疗药物,小分子抑制剂、双抗、单抗、ADC等靶向药物的临床试验正在进行中。
正在招募肺癌、食管癌、肝癌、胃癌、结直肠癌、宫颈癌、卵巢癌、乳腺癌、胆管癌、子宫内膜癌、黑色素瘤、肉瘤、恶性血液疾病、淋巴瘤等各种恶性肿瘤,想要了解或者参加临床试验项目,可以咨询我们医学部的老师。

参考文献
[1] Maccaroni, Elena et al. “BRCA mutations and gastrointestinal cancers: When to expect the unexpected?.” World journal of clinical oncology vol. 12,7 (2021): 565-580.
[2]Moore, Kathleen et al. “Maintenance Olaparib in Patients with Newly Diagnosed Advanced Ovarian Cancer.” The New England journal of medicine vol. 379,26 (2018): 2495-2505.
[3] Pujade-Lauraine, Eric et al. “Olaparib tablets as maintenance therapy in patients with platinum-sensitive, relapsed ovarian cancer and a BRCA1/2 mutation (SOLO2/ENGOT-Ov21): a double-blind, randomised, placebo-controlled, phase 3 trial.” The Lancet. Oncology vol. 18,9 (2017): 1274-1284.
[4] González-Martín, Antonio et al. “Niraparib in Patients with Newly Diagnosed Advanced Ovarian Cancer.” The New England journal of medicine vol. 381,25 (2019): 2391-2402.
[5] Mirza, Mansoor R et al. “Niraparib Maintenance Therapy in Platinum-Sensitive, Recurrent Ovarian Cancer.” The New England journal of medicine vol. 375,22 (2016): 2154-2164.
[6] Coleman, Robert L et al. “Rucaparib maintenance treatment for recurrent ovarian carcinoma after response to platinum therapy (ARIEL3): a randomised, double-blind, placebo-controlled, phase 3 trial.” Lancet (London, England) vol. 390,10106 (2017): 1949-1961.
[7] Herencia-Ropero A, Llop-Guevara A, Staniszewska AD, et al. The PARP1 selective inhibitor saruparib (AZD5305) elicits potent and durable antitumor activity in patient-derived BRCA1/2-associated cancer models. Genome Med. 2024;16(1):107.
[8] Bazan Russo, T.D., Mujacic, C., Di Giovanni, E. et al. Polθ: emerging synthetic lethal partner in homologous recombination-deficient tumors. Cancer Gene Ther 31, 1619–1631 (2024).
[9]Wethington SL, Shah PD, Martin L, et al. Combination ATR (ceralasertib) and PARP (olaparib) Inhibitor (CAPRI) Trial in Acquired PARP Inhibitor-Resistant Homologous Recombination-Deficient Ovarian Cancer. Clin Cancer Res. 2023;29(15):2800-2807.
[10]Drew Y, Kim JW, Penson RT, et al. Olaparib plus Durvalumab, with or without Bevacizumab, as Treatment in PARP Inhibitor-Naïve Platinum-Sensitive Relapsed Ovarian Cancer: A Phase II Multi-Cohort Study. Clin Cancer Res. 2024;30:50-62.
[11] Kathleen N, Moore,Antoine, Angelergues,Gottfried E, Konecny et al. Mirvetuximab Soravtansine in FRα-Positive, Platinum-Resistant Ovarian Cancer.[J] .N Engl J Med, 2023, 389: 2162-2174.