滤泡性淋巴瘤客观缓解率96%,艾可瑞妥单抗已纳入上市申请优先审评品种名单,多个不同疗法的滤泡性淋巴瘤临床试验进行中
截至2024年9月21日,中位随访时间28.2个月,在108例可评估疗效患者中,客观缓解率(ORR)为96%,完全缓解率(CR)为88%。
对于高危亚组,原发性难治患者CR率为90%,双重难治(抗CD20 + 烷化剂)组为82%,POD24(一线治疗24个月内疾病进展)组为83%。2年持续CR率为82%,无进展生存(PFS)率为76%,总生存(OS)率为90%,未启动下一线治疗的患者为84%,微小残留病(MRD)阴性率为86%。
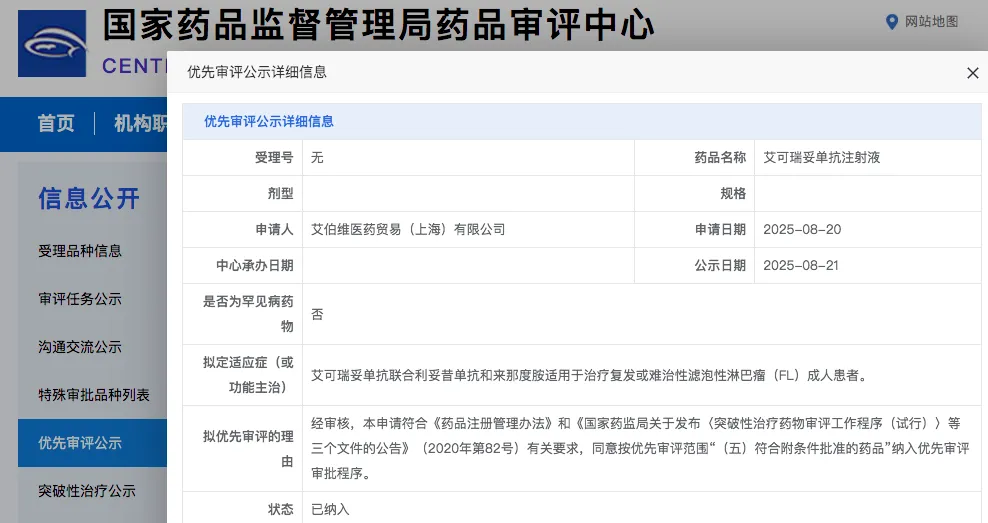


在CDE官网显示[2],一项评价RJMty19注射液(CD19-CAR-DNT细胞药)治疗复发/难治性B细胞非霍奇金淋巴瘤受试者的耐受性、安全性和有效性的开放、单臂I期临床试验正在进行中,招募非霍奇金淋巴瘤(滤泡性淋巴瘤)患者参加,若有需要,可咨询医学部老师。

RJMty19注射液(主要活性成分为CD19-CAR-DNT细胞)由广东瑞顺生物技术有限公司基于人源化CD19-CAR全球专利开发的一款全球创新现货通用型第二代DNT细胞治疗产品[4]。
接受中高剂量组单次给药的7例患者中,第28天PET-CT结果显示客观缓解率(ORR)为71.4%(5/7),完全缓解率(CRR)为28.6%(2/7),最长缓解持续时间为9.79个月。
在已接受多次给药的3例患者中,客观缓解率(ORR)为100%(3/3),完全缓解率(CRR)为67%(2/3)。
参与临床试验的患者,可以免费用试验新药,与试验相关的检查也是免费的。
目前有CAR-T、TIL等细胞疗法,PD-1/PD-L1等免疫治疗药物,小分子抑制剂、双抗、单抗、ADC等靶向药物的临床试验正在进行中。
正在招募肺癌、食管癌、肝癌、胃癌、结直肠癌、宫颈癌、卵巢癌、乳腺癌、胆管癌、子宫内膜癌、黑色素瘤、肉瘤、恶性血液疾病、淋巴瘤等各种恶性肿瘤,想要了解或者参加临床试验项目,可以咨询我们医学部的老师。

参考文献:
2.国家药品监督管理局药品审评中心(CDE)官网.
3.格博生物新型分子胶降解剂GLB-002获批临床试验,格博生物官方微信公众号,文章发布于2023年10月8日.